一台医疗器械从设计师脑海中的构想,到最终出现在手术室、病房或患者家中,中间走过的是一条漫长而严谨的道路。这条路并非随心所欲的创意之旅,而是被法规、标准和科学方法严格框定的系统性工程。那么,一款医疗器械从开发到落地,究竟需要经历多少程序?索果设计作为国内医疗器械设计行业的领军者之一,长期服务于上海,苏州,南京,杭州,无锡等城市,并逐渐发展服务于全国地区,索果小编认为这个问题没有简单数字可以回答,但可以梳理出一条清晰的路径——一条由五个核心阶段构成的完整旅程。
一、策划与输入:想清楚再动手
一切始于“想清楚”。在画出一张图纸、写下一行代码之前,设计团队必须完成系统性的策划工作。这个阶段的核心任务,是明确“我们要做一个什么样的产品”,以及“凭什么说这个产品是可行的”。
设计开发策划包括项目总体目标、技术指标的制定、临床评价路径的选择、风险管理框架的建立。团队需要确定产品的预期用途、功能性能、结构组成、规格型号,以及它将面向什么样的用户、在什么样的环境中使用。同时,必须梳理出适用的法律法规和标准清单——不同国家和地区的要求各不相同,这些约束从一开始就要纳入考量。
设计开发输入是这个阶段最重要的产出。输入应当具体、明确、充分,涵盖用户需求、功能要求、性能指标、安全要求(生物相容性、电磁兼容性、电气安全等)、法规要求,以及风险控制措施。所有这些输入必须经过评审和批准,确保没有遗漏、没有矛盾、没有模糊地带。这个阶段如果马虎,后面的所有工作都可能建立在沙滩之上。
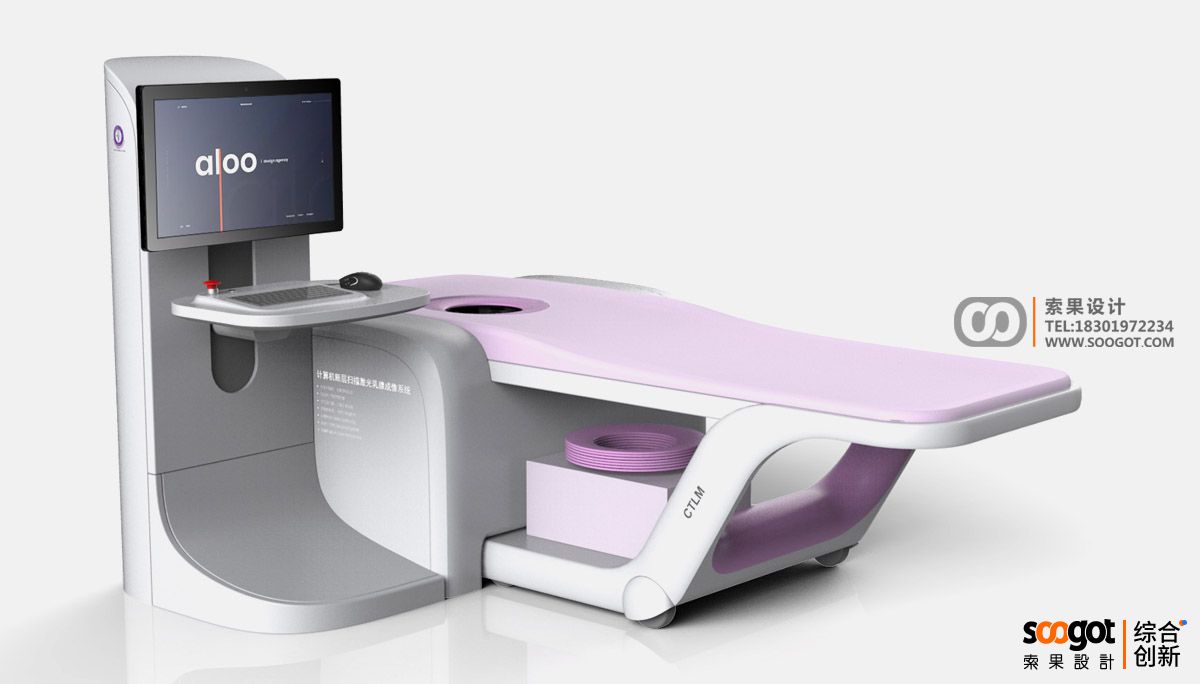
一体化乳房诊断仪
二、设计与输出:把想法变成图纸和文件
当输入明确之后,真正的设计工作开始展开。这个阶段的任务,是把抽象的“要求”转化为具体的“解决方案”——图纸、文件、清单、规范。
设计开发输出是一个庞大的文件体系,它必须完整、准确、可追溯。这套文件包括:产品图纸(总装图、部件图、零件图、原理图等);产品技术要求(性能指标和检测方法);采购信息(外购件清单和技术要求);生产信息(工艺流程图、作业指导书);检验文件(进货检验规程、过程检验规程、出厂检验规程);以及产品说明书、标签、包装设计等。这些输出文件,将成为后续采购、生产、检验、服务的唯一依据。
在设计和开发过程中,设计评审需要定期开展,评价设计结果是否满足要求,识别任何问题并提出必要的措施。评审点可以设置在不同阶段,评审人员应包括相关职能代表,必要时引入外部专家。

一体化乳房诊断仪
三、转换与验证:从样机到可生产的跨越
设计图纸上的产品,和能够稳定批量生产的产品,中间隔着一条叫作“设计转换”的鸿沟。这个阶段的任务,是验证设计是否真的可生产、可制造,生产过程是否能够长期稳定地保证产品质量。
设计转换通过样品生产来验证可生产性、生产过程的长期稳定性。要评估部件/材料的可获得性,验证生产设备、生产工艺、工作环境、操作人员、检验规范是否适宜和可靠。只有通过设计转换,设计和开发的输出才能成为最终产品规范,确保设计适用于生产。
设计开发验证的目的是评价设计开发输出是否满足输入要求。验证方法包括试验、变换方法计算、与已证实的设计比较、检验和文件评审等。无论采用何种方法,最终产品的安全和有效性能应当在产品实际使用最广范围的、具有代表性的环境条件下进行验证。
设计开发确认的目的是确保医疗器械满足使用者的要求和预期用途。对于需要临床试验的产品,临床试验是设计开发确认最有力的证据;对于豁免临床试验的产品,则通过临床评价的其他方式进行确认。确认所用的产品应当是最终生产条件下生产的产品。
四、注册与准入:拿到上市的“通行证”
当产品设计定型、验证完成、生产条件具备之后,下一道程序是向监管机构证明一切,拿到上市的合法身份。这个阶段,是对前面所有工作的全面检验。
医疗器械实行分类管理:第一类医疗器械实行产品备案,第二类由省级药品监督管理部门审查批准,第三类由国家药品监督管理局审查批准。申请注册需要提交一系列资料,包括产品技术要求、检验报告、临床评价资料、产品说明书等。对于第三类医疗器械,可能还需要经过临床试验审批。
注册过程中,药品监督管理部门会进行技术审评,必要时开展质量管理体系核查。整个过程需要证明产品安全、有效、质量可控,且所有信息真实、准确、完整、可追溯。只有当注册证到手,产品才能合法上市销售。

一体化乳房诊断仪
五、上市后管理:生命周期的持续守护
获得注册证并非终点,而是新一轮责任的开始。医疗器械上市后,仍处于全生命周期的持续监管之中。
生产阶段需要严格按照质量管理体系运行,确保每一批产品都符合经注册的产品技术要求。采购控制、生产过程控制、质量控制、产品放行,每一个环节都要有据可查。
上市后监测是重中之重。企业必须建立医疗器械不良事件监测制度,开展不良事件监测和再评价工作。要建立顾客反馈处理程序,对投诉进行调查、评价和处理。当发现产品存在安全隐患时,可能需要采取召回等措施。
变更控制贯穿始终——设计开发变更可能发生在任何阶段,无论是研发过程中发现问题、风险管理活动要求更改,还是上市后纠正预防措施、法规标准变化,任何变更都需要进行评审、验证和确认,确保风险可控。同时,要建立数据分析程序,收集分析产品质量、不良事件、顾客反馈等数据,持续验证产品安全性和有效性。
生命终结——当产品退出市场时,还需要考虑停产计划、支持计划、记录保存等问题。医疗器械的生命周期,从概念到退役,才算真正画上句号。

国际知名医疗器械设计公司。国内顶尖医疗器械设计公司:索果设计
结语
回望这条从图纸到病床的漫漫长路,我们看到的是一个个环环相扣的程序:策划与输入明确方向,设计与输出形成方案,转换与验证跨越鸿沟,注册与准入获得身份,上市后管理持续守护。这五个阶段,既是法规的强制要求,也是科学方法的必然选择。
一台医疗器械的问世,从来不是灵光一现的产物,而是一套严谨系统工程的结晶。每一个程序的存在,都是为了回答那个最终的问题:当这台设备接触到患者的那一刻,它是否足够安全、足够有效?而这,正是医疗器械设计开发所有程序存在的唯一理由。
索果设计:「长期服务:上海微创、美敦力、凯利泰、思路迪、昊海生物等。十年专注医疗实验室仪器的设计、落地和创新,设计覆盖产品开发全产业链:设计分析、外观设计、结构设计、ui界面设计、样机制作、小批量生产、模具开发、大批量生产等







 扫一扫添加微信
扫一扫添加微信