很多人以为,设计医疗器械和设计普通产品差不多——画图、开模、生产、上市,几个月搞定。但事实是,一款正经的医疗器械,从最初的一个想法到最终摆在医院里救人,要走过一条漫长且严苛的阶梯。根据《医疗器械生产质量管理规范》,企业必须建立设计开发控制程序,对设计开发的阶段进行划分,并将策划、输入、输出、验证、确认、转换、变更和评审等活动都纳入控制范围。这意味着,整个过程不是在跑步,而是在爬楼梯——每一级都必须踩实了才能往上走。
上海索果设计有限公司深耕长三角设计服务多年,我们深度服务上海、苏州、无锡、南京、杭州、常州等城市,并逐渐发展至全球,熟悉各地产业特点与市场需求,能够为本地企业提供更贴合、更落地的设计方案。从成立至今,十五载匠心沉淀,在创始人张攀的坚持下,秉承着设计好每一款医疗器械设计为目标我们始终以专业立身,让好设计真正走进长三角每一座城市。索果小编把这套流程拆成五大步,逐一说明。
第一步:策划与输入——决定做一台什么样的设备
这一阶段的全部任务,就是搞清楚一个问题:我们要做一台什么样的设备,给谁用,治什么病。听起来简单,但要做的事一点也不少。
团队要完成用户需求文档,明确产品的用户群体、预期用途、使用环境和临床效果预期。接着,把这些笼统的用户需求转化为技术性的、可衡量的设计输入,比如“测量精度±0.1毫米”或“电池续航不少于8小时”。与此同时,法规标准分析必须跟上:列出所有适用的国内外法规,识别产品需满足的具体条款,并制定风险管理计划——按照ISO 14971的要求,组建一个涵盖产品、生产、临床、法规等多领域专家的团队来共同完成。所有这些工作都会被记录在设计开发计划书中,相当于整条开发路线的地图。
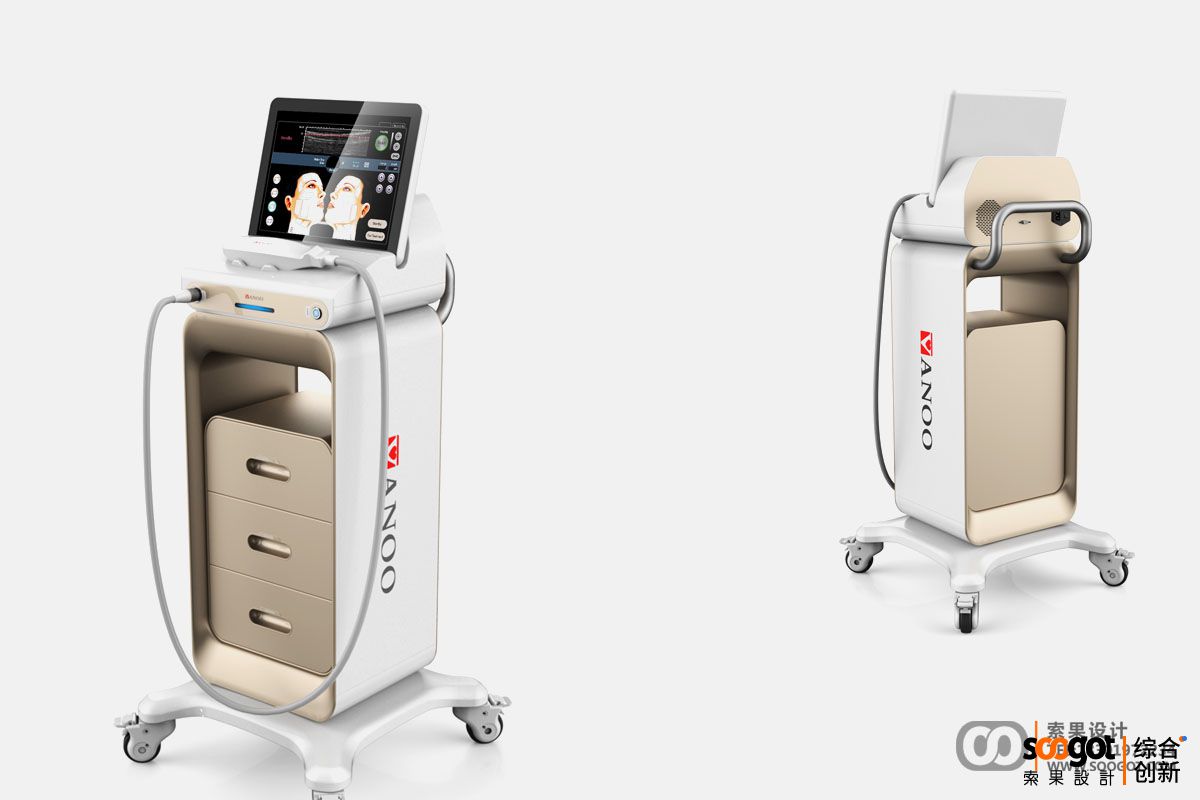
医疗激光治疗仪工业设计
第二步:设计输出——从图纸、代码到实物样机
输入定好了,接下来就是实打实地干。这一阶段的目标,是把纸面上的要求变成实实在在的设计输出——图纸、软件代码、物料清单,以及可供测试的样机。
团队要进行概念设计和详细设计,硬件上要产出原理图、PCB设计、BOM清单,软件上要按风险等级(A/B/C类)搭建架构、编写代码,并进行单元测试。结构设计、工业设计同步推进,通过3D打印或CNC加工制作出原型样机。与此同时,风险管理贯穿始终:设计输入阶段已给出初步的风险控制措施,到了输出阶段,就要验证这些措施是否得到有效执行,确认剩余风险是否可接受。这一阶段的所有输出物,都必须通过评审,确保与设计输入可追溯。
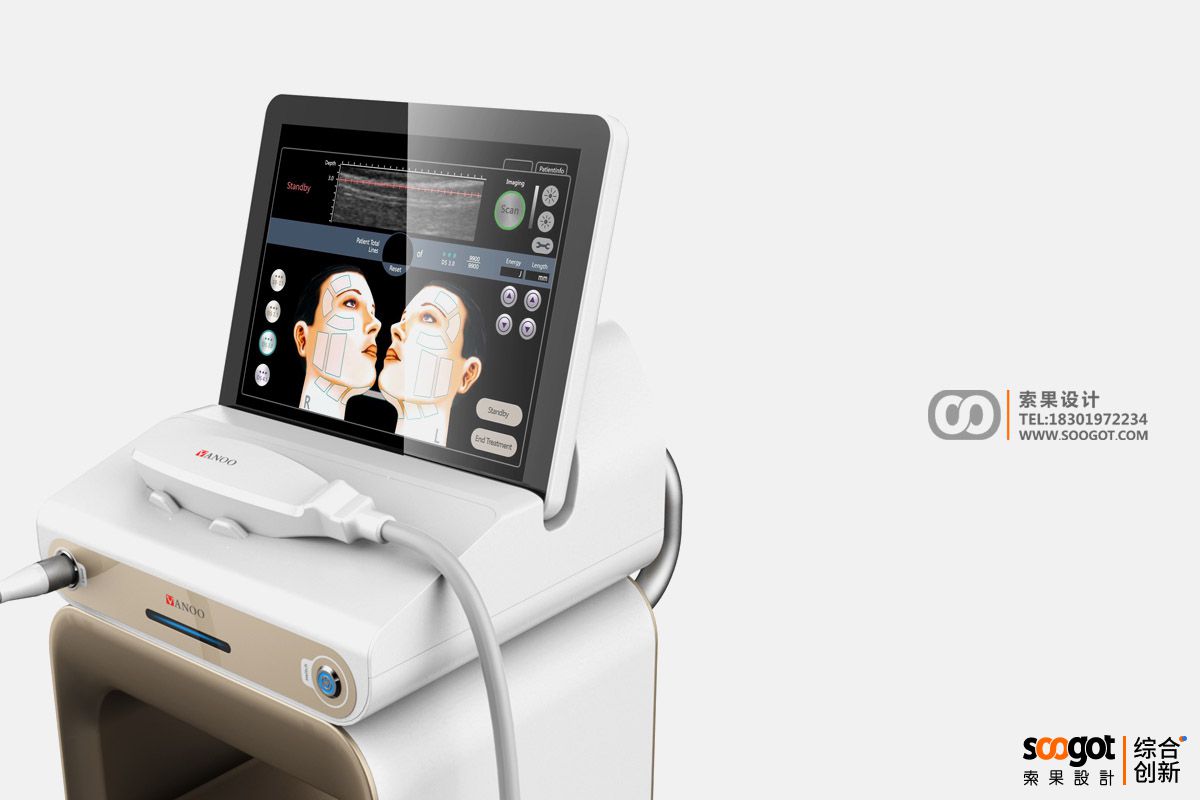
医疗激光治疗仪工业设计
第三步:验证与确认——用数据证明“做对了”且“做了对的东西”
设计做出来了,但还不能欢呼。接下来是验证与确认——说白了就是“魔鬼测试”,用硬数据证明设备靠谱。这一步的目的是评价设计开发输出是否满足规定要求。
验证(Verification) 要回答的问题是:我们做对了设备吗?输出满足输入了吗?具体要做实验室性能测试、电磁兼容性测试(EMC)、环境试验(高温/低温/潮湿/震动)、软件单元测试、集成测试和系统测试,以及材料生物相容性测试等。
确认(Validation) 要回答的问题是:我们做了对的东西吗?设备在真实场景下能满足用户需求吗?这往往是最耗时、最烧钱的环节。团队需要进行临床评价——可能包括非临床研究和临床试验。对于列入免临床目录的产品,可通过同品种医疗器械的临床数据进行评价;否则,需要制定临床试验方案,要通过伦理审查,招募受试者,完成试验后输出临床试验报告。此外,还要根据IEC 62366-1要求完成可用性测试,邀请真实用户操作样机,确保在真实使用场景下,用户不会因设计缺陷而犯错。
第四步:转换、评审与设计历史文件——把研发成果变成可量产的产品
验证和确认通过之后,团队面临最后一道关:从实验室的样机,变成工厂里的量产产品。同时,整个过程的记录必须完整归档,这是法规审查的硬性要求。
设计转换需要把设计图纸、工艺文件、检验标准交给生产线,通过安装确认、运行确认、性能确认来验证生产过程的稳定性。设计评审需要在各关键节点组织评审会议,确保每一阶段的质量可控。最重要的是建立设计历史文件(DHF) ——这不是一堆随便存放的PDF,而是一套结构化的记录集合,必须能证明设计是在严格的设计控制下完成的:涵盖从最初的策划、客户需求、设计输入、设计输出,到设计验证、设计确认、设计评审、设计转换,以及设计变更相关的所有记录。DHF的完整性和可追溯性,是监管机构审查时的重中之重。

医疗激光治疗仪工业设计
第五步:注册申报与上市后监督——拿到“准生证”并持续守护
当所有设计验证、确认和转换工作都完成,设计历史文件齐备后,团队就可以向国家药监局提交注册申报资料,申请医疗器械注册证。这个过程包括提交产品技术报告、风险管理报告、临床评价报告、质量管理体系文件等材料,接受技术审评和可能的体系核查。
需要特别强调的是,医疗器械的生命周期并不是在拿到注册证时就结束了。上市后临床随访(PMCF) 是强制性的:必须将现场数据反馈到开发生命周期中,以触发设计更新、纠正和预防措施或更新的风险评估,从而形成一个真正的循环工程模型。企业还必须建立不良事件报告流程,确保上市后的风险管控不中断。这正是ISO 13485和FDA设计控制所要求的核心理念——始于策划,终于持续改进。

国际知名医疗器械设计公司,国内顶尖医疗器械设计公司:索果设计
结语
设计一款医疗器械的步骤,不是三五个,而是几十上百个相互咬合的动作。从策划输入、设计输出,到验证确认、转换评审,再到注册上市和上市后监督——每一步都有法规要求,每一步都必须留下可追溯的证据。但正是这种“繁琐”,确保了躺在手术台上的患者,面对的不是一件“差不多能用”的机器,而是一台经过了千锤百炼、证据链完整可靠的医疗器械。这套流程,不是束缚创意的枷锁,而是守护生命的铠甲。
“值”。这种多维度的满意,才是大型医疗设备设计的终极目标。
索果设计:「长期服务:上海微创、美敦力、凯利泰、思路迪、昊海生物等。十年专注医疗实验室仪器的设计、落地和创新,设计覆盖产品开发全产业链:设计分析、外观设计、结构设计、ui界面设计、样机制作、小批量生产、模具开发、大批量生产等
下一篇:最后







 扫一扫添加微信
扫一扫添加微信