医疗器械设计是融合医学、工程学与材料科学的复杂系统工程,其设计缺陷可能导致严重临床事故。FDA数据显示,2018-2023年间,因设计问题引发的医疗器械召回事件中,61%源于人机交互缺陷,24%与材料失效相关。索果小编基于ISO 13485质量管理体系,结合人因工程学与前沿技术,系统阐述医疗器械设计必须关注的五大核心维度。
一、安全性与生物相容性设计
1. 材料选择与处理
生物相容性验证:直接接触人体的材料需通过ISO 10993系列测试(细胞毒性、致敏性、植入反应等),其中细胞存活率需>80%(MTT法)
化学稳定性控制:可浸出物含量符合USP<87>标准,塑化剂迁移量<0.1μg/cm²(GB/T 16886.17)
表面处理技术:植入物表面粗糙度Ra≤0.8μm(ASTM F2791),钛合金需经微弧氧化处理形成5-10μm生物活性层
2. 物理安全防护
机械风险防控:锐角倒圆半径≥3mm(IEC 60601-1),动态部件设置双重锁定机制(失效概率<10⁻⁶)
灭菌耐受性设计:高温蒸汽灭菌部件耐受134℃×200次循环(ISO 17665),材料热变形温度>150℃
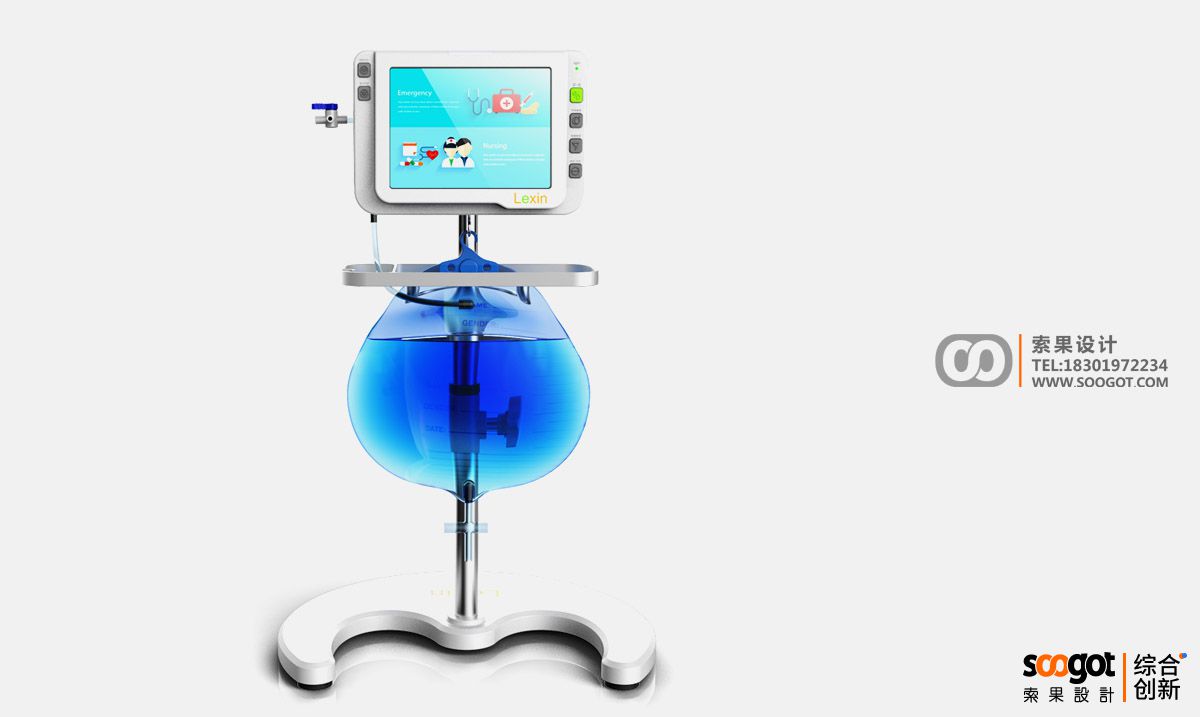
尿动力检测仪产品外观工业设计
二、法规与标准的全面遵循
1. 全球认证体系适配
区域法规差异管理:美国FDA 510(k)需证明实质等效性,欧盟MDR要求临床评价报告(CER),中国NMPA强制人因工程研究
标准转化实施:电气安全执行IEC 60601-1第三版,EMC符合YY 0505-2012,风险管理遵循ISO 14971:2019
文档可追溯体系:建立DHF(设计历史文档)与DMR(设备主记录),满足21 CFR Part 820要求
2. 全流程风险管理
FMEA工具应用:量化评估失效模式,关键风险控制至ALARP(合理可行最低)水平
数字孪生验证:通过虚拟测试覆盖98%使用场景,西门子CT机架完成10万次旋转模拟
三、人机交互与用户体验优化
1. 人机工程学适配
操作界面设计:高频功能键布局在拇指热区(距虎口≤60mm),信息层级≤3层(Hick-Hyman定律)
人体测量学适配:手持器械直径28±3mm(亚洲人群),表面摩擦系数0.4-0.6(ASTM D1894)
多模态反馈:触觉反馈频率20-500Hz可调(精度±2Hz),视觉警示色符合DICOM标准
2. 极端环境适配
抗震与密封设计:通过MIL-STD-810G振动测试(5-500Hz/3.5Grms),防护等级达IP67(IEC 60529)
温湿度耐受:在-40℃至70℃、湿度95%环境中性能波动<1%(IEC 60068-2-30)
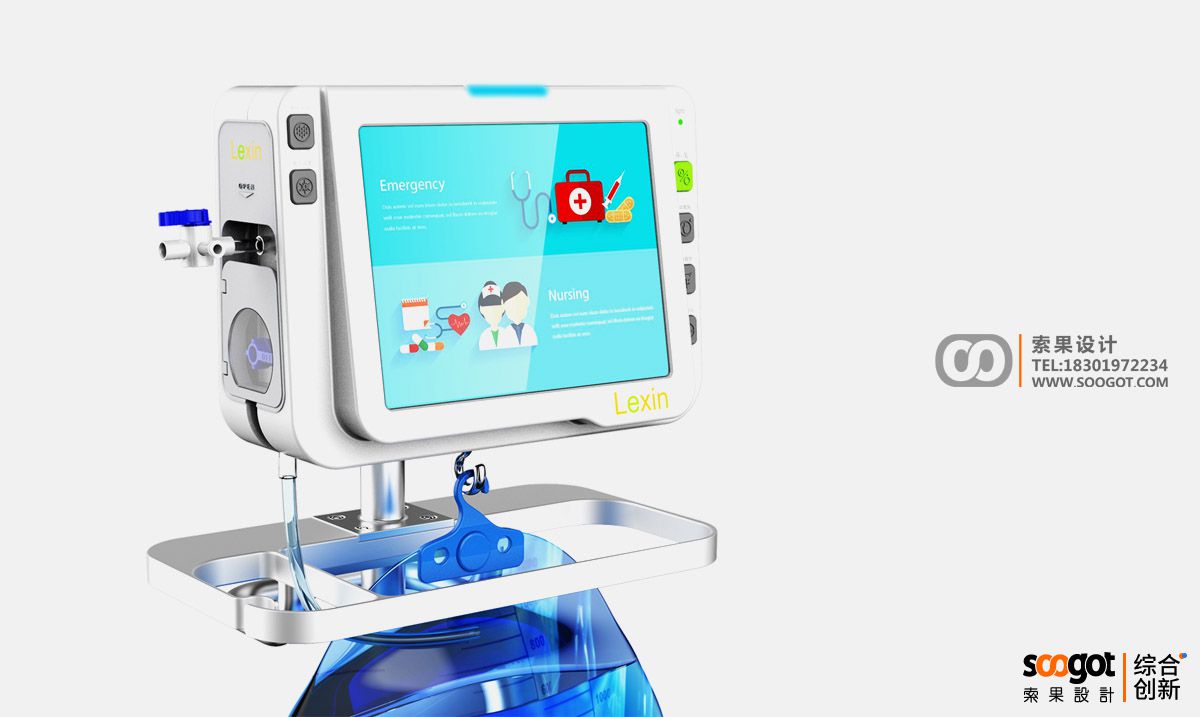
尿动力检测仪产品外观工业设计
四、功能可靠性与精准性保障
1. 核心性能控制
精度验证体系:微创器械定位误差≤0.1mm(ISO 1101),介入导管转向精度≤0.5°,血糖仪误差±0.2mmol/L(ISO 15197)
稳定性测试:加速老化模拟5年使用(ASTM F1980),性能衰减<10%,MTBF>10万小时
2. 智能技术集成
AI辅助系统:影像诊断算法AUC值≥0.95(如联影uAI肺结节检测灵敏度99.2%)
实时监测能力:可穿戴设备采样率≥100Hz,ECG噪声抑制>60dB(IEC 60601-2-47)
五、可持续性与全生命周期管理
1. 绿色材料与工艺
生物基材料应用:使用30%再生PEEK(碳足迹降40%),PLA降解周期≤24个月(ISO 14855)
低碳制造技术:3D打印材料利用率从30%提至95%(EBM工艺),纳米涂层延长寿命3倍
2. 循环经济体系
模块化架构:飞利浦超声探头标准化接口设计,部件更换时间从2小时缩至15分钟
回收技术突破:贵金属电化学回收率>99.9%,美敦力年回收铂族金属200kg
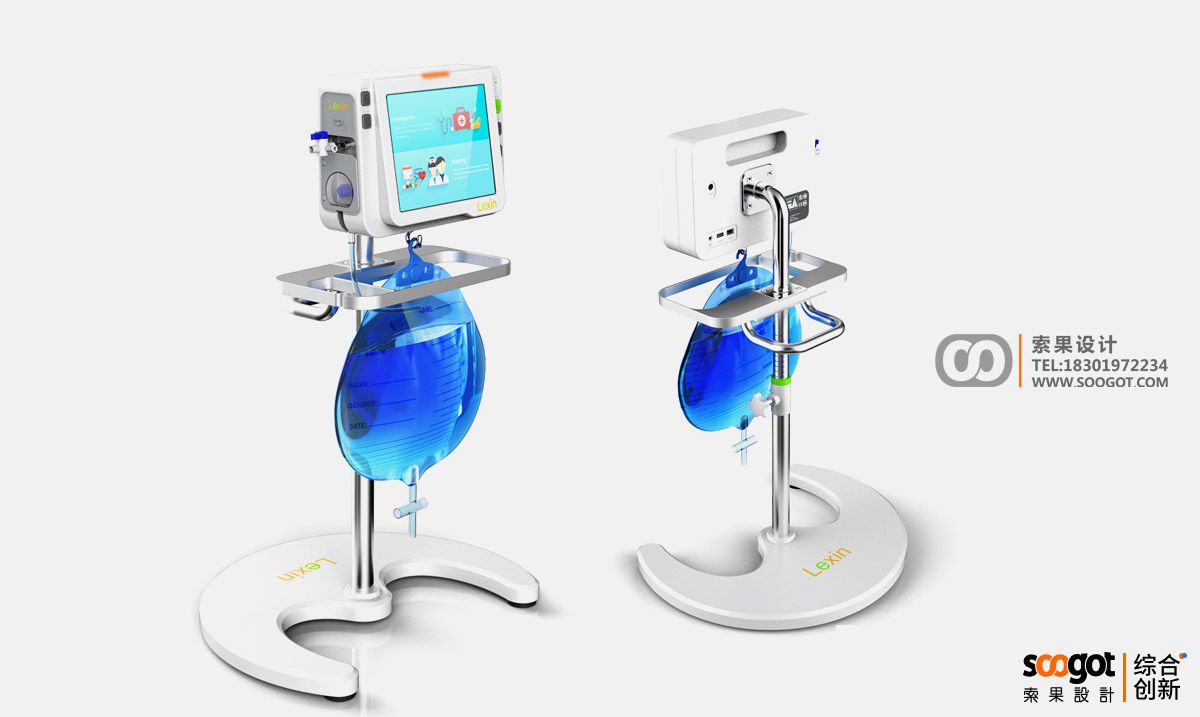
尿动力检测仪产品外观工业设计
结语
医疗器械设计正经历三大技术革命:①柔性电子使可穿戴设备厚度突破0.1mm;②量子传感实现单分子检测;③数字孪生压缩开发周期至传统1/3。未来需在智能化(脑机接口延迟<10ms)、个性化(3D打印假体精度20μm)、绿色化(生物基材料占比>50%)方向突破,同时坚守安全底线。通过ISO/TR 24971等指南构建技术伦理框架,最终实现医疗创新与人类健康的协同进化。
索果设计:「长期服务:上海微创、美敦力、凯利泰、思路迪、昊海生物等。十年专注医疗实验室仪器的设计、落地和创新,设计覆盖产品开发全产业链:设计分析、外观设计、结构设计、ui界面设计、样机制作、小批量生产、模具开发、大批量生产等







 扫一扫添加微信
扫一扫添加微信